2. 실험 이론
(1) 반응기의 종류
(2) CSTR 방정식
(3) Macroscopic Mass Balance
(4) 전도도의 측정
3. 실험 장치 및 준비물
4. 실험방법
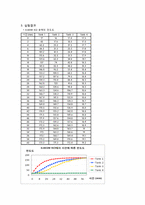
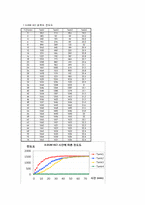
5. 실험결과
6. 결과값의 고찰
(1) 시간에 따른 각 반응의 전도도를 plot한다.
(2) 유량과 염화칼륨을 변수로 했을 때의 전도도 변화를 plot한다.
(3) 위의 결과를 종합해 화학반응에 미치는 영향을 고찰해 본다.
(4) 반응기의 종류를 열거하고 그 특징을 간략하게 설명하시오.
① Power S/W 10 순수토크
② Speed Controller 11 KCl 용액탱크
③ Selector S/W 12 폐수탱크
④ 전도도계 13 Dead time coil
⑤ 유량계 14 농도 측정 센서
⑥ Stirred 15 Header reservoir
⑦ 배수밸브 16 직렬탱크
⑧ 순수공급 펌프 17 농도측정용 전도도계
⑨ KCl 용액 공급 펌프
교반장치, 0.001M KCl 용액, 0.005M KCl 용액, 초시계, 증류수
4. 실험방법
① 0.001M KCl 용액을 만든다.
② A 용기에 20L 순수한 증류수를 넣고 B용기에 0.001M 농도의 KCl용액 10L를 넣어 펌프와 연 결한다.
③ 탱크 1, 2, 3, 4번의 증류수 전도도 값이 일정하게 될 때까지 배관과 탱크를 증류수로 세척하며 빠른 세척을 위해서 교반기를 틀어준다.
④ 교반기 S/W를 올려주고 유량조절기로 알맞은 속도로 유지시켜준다. (233rpm)
⑤ A용기의 증류수를 1,2,3,4번의 탱크에 채운다. (A pump S/W On)
⑥ 탱크 4번으로 Drain 되면 KCl용액을 100cc/min 으로 주입한다.
⑦ 2분 간격으로 탱크 1, 2, 3, 4번의 전도도 값을 기록한다.
⑧ 측정한 값을 그래프로 작성한다.
⑨ KCl 용액을 0.01M 농도로 바꾼 후 위의 과정을 반복한다.








 분야
분야