2. 아황산 분석법
3. 출처
무색 투명한 수용액, 자극적 냄새
이산화황(SO2 )을 물에 녹이면 즉시 얻을 수 있는 산
사진의 현상약, 식품 · 섬유 등의 표백제로 사용
채소 건조 시 효모의 활성 저해 →갈변현상 방지
미생물에 의한 부패 방지
표백과 보존
항 산화 및 환원
액체검체 1~2g 혹은,고체검체 1~2g+물 10ml
↓
삼각플라스크에 넣고 잘 섞어줌
↓
25% 인산 5ml
↓
요오드산칼륨전분지를 달아 맨 콜크마개로 막음
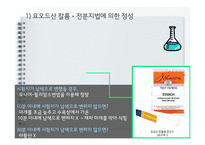
시험지가 남색으로 변했을 경우,
모니어-윌리암스변법을 이용해 정량
10분 이내에 시험지가 남색으로 변하지 않으면?
마개를 조금 늦추고 수욕상에서 가온
10분 이내에 남색으로 변하지 X → 재차 마개를 막아 식힘
30분 이내에 시험지가 남색으로 변하지 않으면?
아황산 X
H2SO3 → H2O + SO2(g)↑ (Decomposition)
산성조건에서 아황산염류가 분해될 때 가스상태의
이산화황 발생
SO2(g) + H2O2 → 2H+(aq) + SO42−(aq) (Oxidation)
과산화수소를 사용하여 산화
2H+(aq) + 2NaOH → 2Na++ 2H2O (Titration)
생성된 수소이온농도를 정량
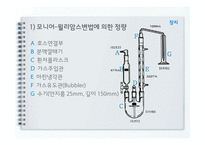
A 호스연결부
B 분액깔때기
C 환저플라스크
D 가스주입관
E 아린냉각관
F 가스유도관(Bubbler)
G 수기(안지름 25mm, 깊이 150mm)
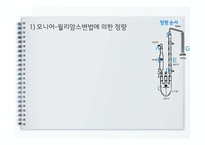
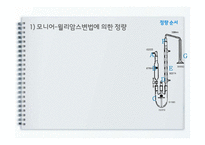
플라스크(C)에 물 400ml, 4N 염산용액 90ml 첨가
냉각기(E)에 물 공급
가스주입관(D)에 질소가스를 0.21l/분의 속도로 통과시키고, 수기(G)에 3% 과산화수소용액 30ml첨가
15분 후 검체 50g을 취해, 5% 에탄올용액 100ml와 혼합
혼합액 수 ml가 남을 때까지 플라스크(C)에 주입 후 1시간 45분 가열
3% 과산화수소용액 소량을 수기(G)에 넣고 0.01N 수산화나트륨 용액으로 적정
공식에 따라 이산화황의 양을 산출 (10ppm미만은 불검출로 함)


















 분야
분야