2. 실험원리
3. 시약 및 기구
4. 실험방법
5. 결과
6. 고찰
7. 참고문헌
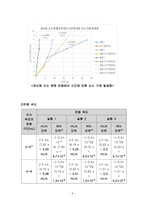
과산화수소가 물과 산소로 분해되는 반응의 속도 상수와 반응차수를 결정하고 화학 반응의 속도에 영향을 주는 인자를 알아본다.
※주의사항
① H2O2를 넣자마자 syringe를 일정한 간격으로 톡톡 친다.
② Syringe의 피스톤을 너무 꽉 넣지 않도록 주의한다.
③ Syringe를 치자마자 1 mL 보다 더 올라갔을 경우, 그 눈금부터 2 mL씩 잰다.
④ Tube가 양쪽 끝까지 들어가도록 끼운다.
5.실험원리
1)화학 반응의 열역학적 해석과 속도론적 해석
수소(H2)와 산소(O2)는 반응하여 물(H2O)를 만들어낸다. 25℃인 용기에 1기압의 수소 기체와 1기압의 산소 기체가 섞여있을 때, 1몰의 물이 만들어지는 반응의 반응 엔탈피는 -286 kJ/mol로 발열 반응이다. 수소와 산소가 반응하면 큰 열이 발생하는 것은 확인할 수 있지만 용기에서 물이 생성되는 것은 관찰할 수 없다.
② 일반화학실험, 자유아카데미, 이홍인 저자, 2016.07.10 발행, P.171 - 반응 경로와 에너지 그래프
③ http://msds.kosha.or.kr/kcic/msdsdetail.do - Dihydrogen dioxide (2018-08-17 개정), (2018-09-13 검색)
④ http://msds.kosha.or.kr/kcic/msdsdetail.do - Potassium iodide(aq) (2018-04-02 개정), (2018-09-13 검색)
⑤ https://blog.naver.com/iup123/100163418670 - 촉매에 따른 활성화 에너지 그림 (2018-09-16 검색)
⑥ https://terms.naver.com/entry.nhn?docId=1147151&cid=40942&categoryId=32251 - 촉매 (2018-09-16 검색)
⑦ http://msds.kosha.or.kr/kcic/msdsdetail.do - Manganese dioxide (2018-04-02 개정), (2018-09-16 검색)
⑧ https://terms.naver.com/entry.nhn?docId=2288274&cid=60227&categoryId=60227 - 반응 속도 상수 (2018-09-16 검색)
기본적인 개념과 실험 이론들도 정리했고,
결과 처리 과정도 자세히 나와있습니다.
또한 엑셀 그래프도 첨부되어 있습니다.











 분야
분야