교사는미리 뜨거운 물을 준비한다.
털실로감을때백반결정가루를박아놓으면결정을잘 얻을 수 있다.
여러 가지의 진한 용액에서 결정을 만들어 볼 수 있다.
실험 준비하기
온도에 따른 용해도의 차이와 포화 용액에 대해 알기.
-온도에 따라 물질이 녹는 양이 다름을 알고 포화 용 액의 개념을 안다.
여러 물질들을 뜨거운 물에 녹인 진한 용액을 식히거 나 증발시키면 어떤 현상이 일어날지 예상해 본다.
실험시 주의점에 대해 이야기해 본다.
1. 유리잔 안의 마술꽃의 원리
요소 용액은 시간이 지남에 따라 증발하게 되고 요소 결정이 생기는데 처음 생긴 요소 결정은 유리잔 바닥에 남아있는 요소 용액을 빨아올리게 된다. 즉, 유리잔에 붙어 있는 요소 결정이 일종의 모세관 역할을 하는 것이다. 모세관 현상에 의해 올라온 용액은 요소 결정 끝에서 다시 증발하여 결정을 계속 만들게 되어 결국엔 유리잔 위까지 넘쳐 만발한 꽃처럼 보이게 된다.
2. 용해도
물에는 설탕이 얼마나 용해될 수 있을까? 에탄올에는 소금이 얼마나 용해될 수 있을까? 용해 도란 어떤 온도에서 용매 100g 속에 최대로 녹아 있는(포화 상태인) 용질의 g 수를 말한다. 용 해도는 용질의 종류와 온도에 따라 용해도가 달라진다. 또한 용매가 어떤 것이냐에 따라서도 용해도가 달라진다.
3. 용해도 곡선
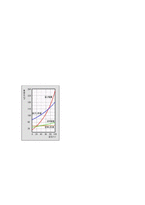
물질의 용해도는 온도의 변화에 따라서 달라지는데, 고체의 용해도는 온도가 상승함에 따라 증가하는 경우가 대부분이다. 이 때, 물질의 용해도와 온도와의 관계를 나타낸 그래프를 용해도 곡선이라고 한다. 왼쪽은 몇 가지 고체들의 용해도 곡선 예이다.
(소금의 경우 온도에 따른 용해도 차이가 거의 없다. 이런 이유로 소금결정을 얻을 때는 냉각이 아닌 물의 증발에 의해 얻게 된다)
4. 포화불포화과포화 용액
① 포화 용액:일정한 온도에서, 더 이상 용해될 수 없는 한계까지 녹아 있는 최대량의 용질을 포함한 용액이다. 즉, 용매 100g에 용질이 용해도만큼 녹아 있는 용액을 포화 용액이라 한다.
② 불포화 용액:일정한 온도에서, 용매 100g에 용질이 용해도보다 적게 녹아 있는 용액을 불포 화 용액이라고 한다. 용질이 더 녹을 수 있는 용액, 즉 포화 상태에 이르지 못한 용액이다.
③ 과포화 용액:불포화 용액과는 반대의 의미로, 포화 상태보다 더 많은 용질이 녹아 있는 경 우이다. 불안정한 용액이므로 이 용액을 흔들거나 또는 용기의 벽을 유리 막대로 문지르면 갑자기 과잉으로 녹아 있던 용질이 석출된다.
-포화불포화과포화 용액을 용해도 곡선에서 찾아볼 수 있다. 다음 용해도 곡선에서 용액 B 와 같은 용해도 곡선에 있는 용액은 t℃에서 포화 상태, 용액 A와 같이 용해도 곡선의 위쪽에 있는 용액은 t℃에서 과포화 상태, 또 용액 C와 같이 용해도 곡선의 아래쪽에 있는 용액은 t℃ 에서 불포화 상태를 나타낸다.
5. 재결정
80℃ 물 100g에 녹인 질산칼륨의 포화 용액에는 질산칼륨이 169g 녹아 있다. 이 용액을 20℃로 냉각시키면 어떤 변화가 일어날까? 20℃에서 질산칼륨의 용해도는 31.6이므로 31.6g보다 더 많이 녹아 있던 질산칼륨은 용액에 녹아 있지 못하고 용액 밖으로 석출될 것이다. 169 - 31.6 = 137.4g의 질산칼륨이 석출된다. 질산칼륨과 같이 용해도가 온도에 따라 크게 변하는 물질의 포화 용액을 높은 온도에서 만든 다음, 이 용액을 냉각시키면 용질이 순수한 결정으로 석출되어 나오는데, 이를 재결정이라고 한다.
그러나 염화나트륨과 같이 온도에 따른 용해도의 변화가 작은 물질은 재결정시 석출되는 양이 아주 적으므로, 염화나트륨의 결정을 얻으려면 가열하여 수용액의 물을 증발시킨다.
※ 평가문항
1. (지식) 백반가루를 온도를 높여가며 녹여보았습니다. 다음 중 맞는 것을 고르세요.
① 더운물보다 찬물에서 더 잘 녹는다.
② 온도를 높였더니 더 많은 양이 녹는다.
③ 용액을 가열했더니 백반가루가 더 이상 녹지 않는다.
④ 용액을 가열하자마자 백반가루가 덩어리져 가라앉기 시작한다.
⑤ 온도를 높일수록 비커 밑바닥에 가라앉는 백반가루가 많아진다.
☞ 답 ②
2. (이해) 백반 결정을 만들 때 모양이 큰 결정을 얻기 위해서는 어떻게 해야 할까요?
① 백반 가루를 조금 넣어 녹인다.
② 찬물에 백반 포화용액이 들어있는 비커를 담근다.
③ 백반 포화용액 비커를 스티로폼 상자에 넣어서 식힌다.
④ 비커를 많이 흔들어 준다.
⑤ 햇빛에 노출시킨다.
☞ 답 ③
3. (탐구) 소금 결정을 얻을 때는 다른 결정에 비해 시간이 오래 걸리는데, 그 이유는 소금 결정 은 포화용액을 식혀서 얻는 것이 아니라 물을 ( )시켜 얻기 때문이다.
☞ 답 : 증발
4. (탐구) 여러 가지 결정들의 크기가 작게 만들어졌습니다. 왜 그럴까요?
① 용질을 너무 많이 넣어 포화용액을 만들었다.
② 포화용액을 식힐 때 얼음물에 넣어서 식혔다.
③ 수건으로 포화용액이 든 용기를 감싸 식혔다.
④ 포화용액의 양을 적게 하여 식혔다.
⑤ 포화용액이 든 용기를 스티로폼 상자 안에 두었다.
☞ 답 ②
5. (탐구) 백반 결정과 소금 결정, 황산구리 결정을 돋보기로 관찰하였습니다. 그 모양과 색깔은 어떠한가요?
① 백반 결정-정육면체 모양-푸른색
② 소금 결정-수정결정 모양-투명한 색
③ 소금 결정-정팔면체 모양-흰색
④ 백반 결정-정팔면체 모양-반투명한 흰색
⑤ 황산구리 결정-수정결정 모양-흰색
☞ 답 ④
6. (응용) 붕산과 소금이 섞여있는 용액이 있습니다. 어떤 방법으로 분리할까요?
① 가열만 하면 분리된다.
② 거름종이로 걸러주면 분리된다.
③ 가열한 후 냉각시키고 거름종이로 걸러준 후, 거른 액을 증발시킨다.
④ 용액에 물을 다량으로 넣어주면 용액이 이층으로 되어 분리된다.
⑤ 가열한 후 용기를 스티로폼 상자에 넣어 며칠동안 놓아둔다.
☞ 답 ③
7. (실험) 포화용액을 담아두는 비커와 페트리 접시는 그 내부표면을 깨끗이 하여 사용해야 합 니다. 그 이유에 대해 말해 봅시다.
☞ 포화용액으로부터 결정을 만들 때 용질이 재결정되어 그것이 결정의 핵이 되어 결정이 커 지게 된다. 그런데 비커나 페트리 접시의 내부표면에 먼지나 때가 있으면 그것이 결정의 핵이 되어 버려 순수한 결정을 얻기 힘들기 때문에 비커나 페트리 접시의 내부표면을 깨 끗하게 한 후 포화용액을 담아야 한다. 또한 용기 내부의 흠도 먼지와 같은 작용을 한다.






 분야
분야