2. 실험 이론
3. 실험 장치
4. 실험 방법
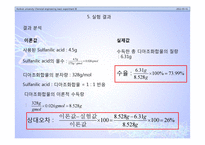
5. 실험 결과
6. 고찰 및 결론
7. 참고문헌
디아조화합물
실험목표
1. 디아조화와 짝지음 반응에 의해 염료를 합성
2. 반응에 미치는 여러가지 조건 검토
3. 저분자물이 고분자화합물에 흡착되는 과정 관찰
(염색을 응용)
1. 디아조화
방향족 1차 아민 + 아질산 (염산 환경) -> 디아조늄 염 + 물
일반적인 방법 :
-아민 1몰 + 10배의 물, 2.5몰의 염산
0℃ 근처에서 교반하면서 아질산소다 수용액을 가함
- Surfanilic acid와 같이SO3H 염을 가지면서 물, 염산에 거의 녹지 않는 아민
: 탄산 소다를 사용하여 녹임->NaNO2를 가하여 디아조화
- 염기성이 극히 적고 염산에 용해되지 않는 아민
: cons H2SO4에 녹여서 nitrosile sulfuric acid를 사용하여 디아조화
◎ 이론적으로 아미노기 한 개에 염산 2당량
1당량은 아질산(HONO)을 생성하기 위해, 나머지 1당량은 방향족 1차 아민을
염으로 만들기 위함.
방향족 1차아민을 염으로 만드는 이유: 디아조늄이온이 방향족아민과 짝지음
반응을 하는 것을 방지
◎ 염산 2몰 X, 2.5몰 O
아질산의 해리를 막고 생성한 아민염의 가수분해 억제, 생성된 디아조늄
염과 원료 아민과의 짝지음 방지
◎ 얼음을 이용해 0℃ 근방에서 처리
디아조늄염은 불안정 – 온도가 높으면 N2가 떨어져나가 치환됨
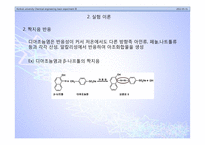
2. 짝지음 반응
디아조늄염은 반응성이 커서 저온에서도 다른 방향족 아민류, 페놀,나트톨류등과 각각 산성, 알칼리성에서 반응하여 아조화합물을 생성
Ex) 디아조늄염과 β-나프톨의 짝지음
실험과정에서 이용되는 이론
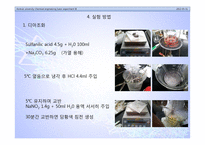
시약A∶ Sulfanilic acid 4.5g+conc HCl 4.4ml+ H2O 50ml + Na2CO3 6.25g
시약B∶ NaNO21.7g+ H2O 8.75ml
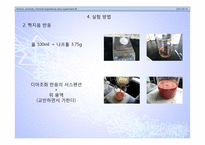
시약C∶ H2O 50ml+나프톨 3.75g
1. 디아조화 과정
[그림 a] 같이 시약A에서 설파닐산을 산성조건에 놓이게 함으로써 SO3기를 가진 물질로 만든다.
시약B를 혼합함으로써 설파닐산을 시약B에 있는 NaNO2와 산성조건에서 반응하게 하여 [그림 b]와 같은 물질을 합성(디아조늄염 생성)
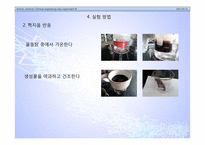
2. 짝지음 반응 과정
시약C를 혼합하면 시약 A, B를 혼합하여 생성된 [그림 b]의 물질과 나프톨이 반응하게 된다.
이것이 반응하여 메틸오렌지∥를 얻게 된다.
유기화학, 자유아카데미
Merck index (MSDS) (한국산업안전공단 인터넷 주소 - http://www.kosha.net/)
http://100.naver.com/100.php?where=100&i=41293
http://kowon.dongseo.ac.kr/%7Eccpark/root/organ/or_ex11_ob.htm
http://kin.naver.com/qna/detail.nhn?d1id=11&dirId=1115&docId=58305509&qb=dHJpYXplbmU=&enc=utf8§ion=kinrank=1&search_sort=0&spq=0&pid=gN6slz331yGsss9hdv4ssv--072042&sid=TcKAdf9nwk0AAA25IsQ








 분야
분야